Tin hóa chất
Thông tin cơ bản hóa chất Kali hydroxit
Kali hydroxi – Quy trình sản xuất, ứng dụng và những lưu ý quan trọng khi sử dụng
Kali hydroxit là một hóa chất công nghiệp có tính ăn mòn cao, được ứng dụng phổ biến trong nhiều lĩnh vực, đặc biệt là trong ngành công nghiệp sản xuất phân bón, hóa mỹ phẩm. Vậy Kali hydroxit là gì, tính chất lý hóa đặc trưng và những ứng dụng quan trọng trong thực tiễn của chúng ra sao? Bài viết dưới đây VIETCHEM sẽ cùng bạn đi giải đáp tất cả những thắc mắc về hợp chất học này!
Kali hydroxit là một bazo mạnh, dễ dàng tác dụng với nước và cacbonic trong không khí để tạp thành Kali cacbonat.
Ở dạng dung dịch, nó có khả năng ăn mòn thủy tinh, vải, giấy, da còn ở dạng chất rắn nóng chảy, nó ăn mòn được sứ, platin.
Thông tin cơ bản
| Potassium hydroxide | |
|---|---|
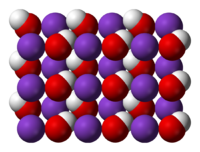
crystal structure of KOH
|
|
| Danh pháp IUPAC | Potassium hydroxide |
| Tên khác | Caustic potash Potash lye Potassia Potassium hydrate |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| Số EINECS | |
| ChEBI | |
| Số RTECS | TT2100000 |
| Ảnh Jmol-3D | ảnh |
| SMILES |
Danh sách[hiện]
|
| InChI | 1/K.H2O/h;1H2/q+1;/p-1 |
| Thuộc tính | |
| Công thức phân tử | KOH |
| Phân tử gam | 56.1056 g/mol |
| Bề ngoài | white solid, deliquescent |
| Mùi | odorless |
| Khối lượng riêng | 2.044 g/cm3[1] |
| Điểm nóng chảy | 406 °C (679 K; 763 °F) |
| Điểm sôi | 1.327 °C (1.600 K; 2.421 °F) |
| Độ hòa tan trong nước | 97 g/100 mL (0 °C) 121 g/100 mL (25 °C) 178 g/100 mL (100 °C)[1] |
| Độ hòa tan | soluble in alcohol, glycerol insoluble in ether, liquid ammonia |
| Độ axít (pKa) | 13.5 (0.1 M) |
| Chiết suất (nD) | 1.409 |
| Cấu trúc | |
| Cấu trúc tinh thể | rhombohedral |
| Nhiệt hóa học | |
| Entanpi hình thành ΔfH |
−425 kJ·mol−1[2] |
| Entrôpi mol tiêu chuẩn S |
79 J·mol−1·K−1[2] |
| Các nguy hiểm | |
| MSDS | ICSC 0357 |
| Phân loại của EU | Corrosive (C) Harmful (Xn) |
| Chỉ mục EU | 019-002-00-8 |
| NFPA 704 |
0
3
1
|
| Chỉ dẫn R | R22, R35 |
| Chỉ dẫn S | (S1/2), S26, S36/37/39, S45 |
| Điểm bắt lửa | Non-flammable |
| LD50 | 273 mg/kg (rat, oral) |
| Các hợp chất liên quan | |
| Anion khác | Potassium hydrosulfide Potassium amide |
| Cation khác | Lithium hydroxide Sodium hydroxide Rubidium hydroxide Caesium hydroxide |
| Hợp chất liên quan | Potassium oxide |
2. Tính chất hóa học của KOH
- Là một bazo mạnh có khả năng làm thay đổi màu sắc các chất chỉ thị như khiến quỳ tím chuyển sang màu xanh, còn dung dịch phenolphtalein không màu thành màu hồng.
- Ở điều kiện nhiệt độ phòng, KOH tác dụng với oxit axit như SO2, CO2
KOH + SO2 → K2SO3 + H2O
KOH + SO2 → KHSO3
- Tác dụng với axit tạo thành muối và nước
KOH(dd) + HCl(dd) → KCl(dd) + H2O
- Tác dụng với các axit hữu cơ để tạo thành muối và thủy phân este, peptit
RCOOR1 + KOH → RCOOK + R1OH
- Tác dụng với kim loại mạnh tạo thành bazo mới và kim loại mới
KOH + Na → NaOH + K
- Tác dụng với muối để tạo thành muối mới và axit mới
2KOH + CuCl2 → 2KCl + Cu(OH)2↓
- KOH là một bazo mạnh, trong nước phân ly hoàn toàn thành ion Na+ và OH–
- Phản ứng với một số oxit kim loại mà oxit, hidroxit của chúng lưỡng tính như nhôm, kẽm,…
2KOH + 2Al + 2H2O → 2KAlO2 + 3H2↑
2KOH + Zn → K2ZnO2 + H2↑
- Phản ứng với một số hợp chất lưỡng tính
KOH + Al(OH)3 → KAlO2 + 2H2O
2KOH + Al2O3 → 2KAlO2 + H2O


